查看与生产过程中任何阶段的无菌失效相关的数据
从 10,000 美元到 100 万美元1
修复无菌失效的潜在费用
静脉用药协会(Parenteral Drug Association)与国际制药工程师协会(ISPE)合作进行了一项基准调查,估计一次药品生产失败的调查费用可能在 10,000 美元到 100 万美元之间。
免责声明和说明
1. Macher J. Business case for quality. Presented at: Pharmaceutical Quality System (ICH Q10) Conference, Arlington, VA, October 4-6, 2011.
2. Perrone M. FDA fines Genzyme $175M for manufacturing problems. San Diego Union-Tribune. https://www.sandiegouniontribune.com/sdut-fda-fines-genzyme-175m-for-manufacturing-problems-2010may24-story.html. Published May 24, 2010. Accessed February 14, 2024.
3. Sutton S, Jimenez L. Am Pharm Rev. 2012;15(1):42-57.
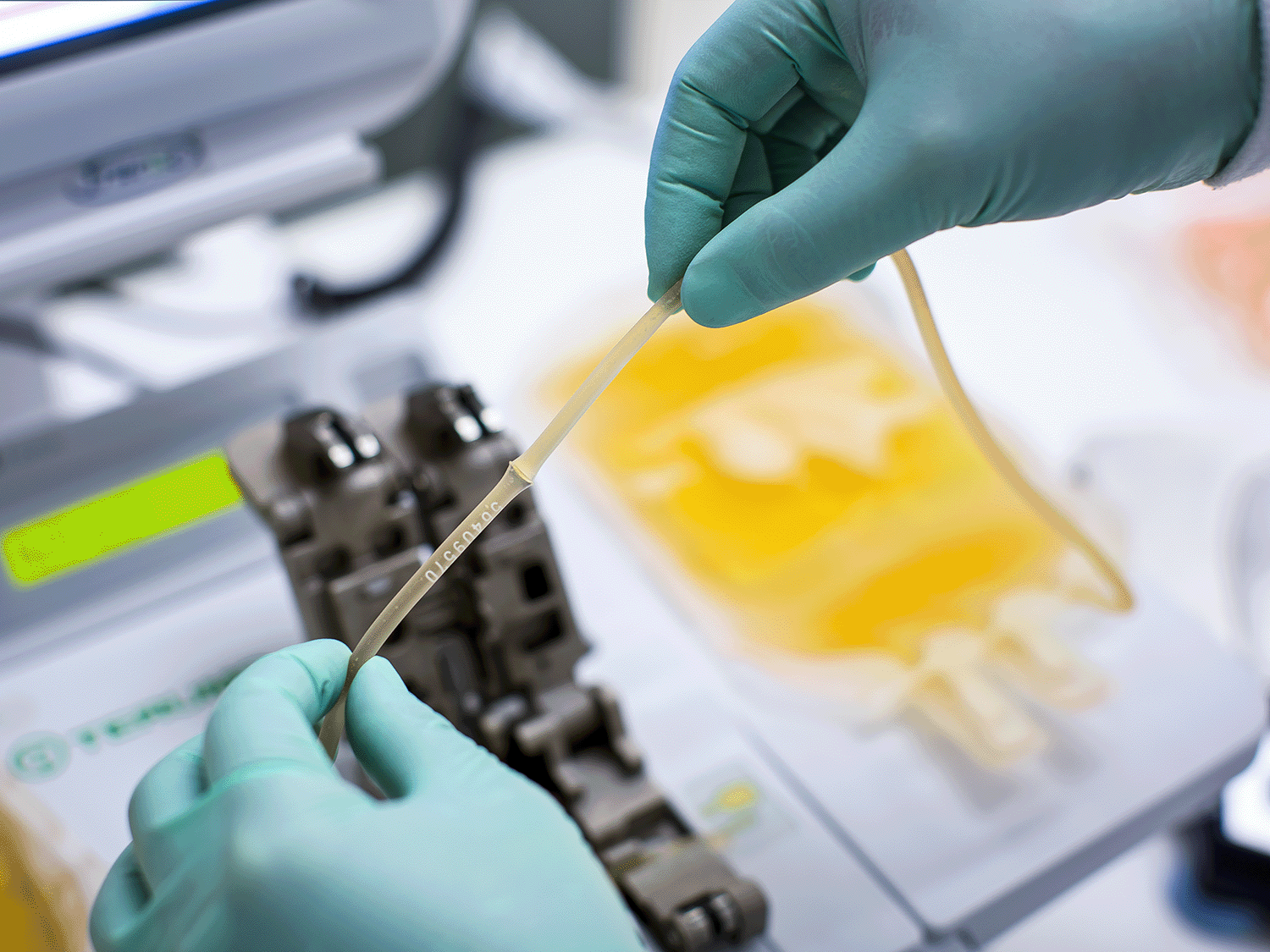
*使用外径(OD)标称值为5.46毫米(0.215英寸)、壁厚为0.84毫米(0.033英寸)的PVC管路,或外径标称值为6.35毫米(0.25英寸)、内径标称值为3.18毫米(0.125英寸)的C-Flex管路。
警告:列出的管路尺寸和类型已由泰尔茂血液与细胞技术公司测试其焊接强度和无菌性;然而,一些用户在使用其他类型的热塑性管路时也取得了成功的结果。PVC和C-Flex管路是可用于该产品的合适管路形式。如果选择使用规格外的管路,您需自行根据所需应用的相关标准测试焊接强度和无菌性。使用非指定管路可能导致低强度或非无菌的焊接。
注意: C-Flex是圣戈班生命科学公司在美国和/或其他国家的注册商标或商标。